Kết quả cho thấy thịt tôm không còn khả năng lây nhiễm sau khi luộc hơn 1 phút.

Bệnh đốm trắng (WSD), do virus gây hội chứng đốm trắng (WSSV) gây ra, hiện là một trong những mối đe dọa nghiêm trọng nhất đối với ngành nuôi tôm toàn cầu. Bệnh có khả năng gây chết rất cao, có thể lên đến 100% đối với các quần thể tôm không mang mầm bệnh đặc hiệu (SPF) trong điều kiện nuôi thương phẩm chỉ sau vài ngày nhiễm bệnh. Virus WSSV lần đầu tiên được ghi nhận tại Đài Loan vào năm 1992 và kể từ đó đã lan rộng ra nhiều khu vực trên thế giới, bao gồm Nhật Bản, Hàn Quốc, Đông Nam Á, Nam Á, khu vực Địa Trung Hải, Trung Đông, châu Mỹ và Úc.
Nguy cơ lây lan WSSV chủ yếu xuất phát từ hoạt động vận chuyển quốc tế các sản phẩm tôm nhiễm bệnh, bao gồm tôm sống, tôm đông lạnh còn đầu (HO), còn đầu và vỏ (HOSO), bỏ đầu và vỏ (HLSO), cũng như các sản phẩm đã qua chế biến. Do nguy cơ vô tình đưa mầm bệnh xâm nhập thông qua hàng hóa thương mại, nhiều quốc gia như Úc, Ả Rập Xê Út và một số nước khác đã áp dụng các quy định nghiêm ngặt nhằm kiểm soát việc nhập khẩu tôm và các sản phẩm tôm tươi sống. Việc sàng lọc nhằm xác định sự hiện diện hoặc vắng mặt của các tác nhân virus thường được thực hiện bằng kỹ thuật phản ứng chuỗi polymerase (PCR). Trong trường hợp lô hàng cho kết quả dương tính, sản phẩm thường bị tiêu hủy hoặc xử lý nhiệt (nấu chín) theo quy định nhằm ngăn chặn nguy cơ lây lan dịch bệnh.
Gần đây, các mẫu tôm đã qua chế biến nhiệt và nhiễm WSSV được ghi nhận cho kết quả dương tính khi phân tích bằng phương pháp phản ứng chuỗi polymerase (PCR). Tuy nhiên, hiện vẫn chưa có nghiên cứu nào xác định rõ khả năng lây nhiễm thực sự của WSSV trong các mẫu tôm nấu chín có kết quả PCR dương tính. Một số nghiên cứu trước đây cho thấy các sản phẩm tôm đông lạnh từng là con đường đưa WSSV xâm nhập vào khu vực châu Mỹ vào năm 1995. Tuy nhiên, chỉ có rất ít công trình khoa học được bình duyệt đề cập đến nguy cơ lây nhiễm WSSV từ tôm thương phẩm đã qua chế biến nhiệt. Đáng chú ý, các nghiên cứu này chủ yếu dừng lại ở việc phát hiện vật liệu di truyền của virus bằng PCR, trong khi chưa làm rõ liệu các trình tự DNA được phát hiện có còn khả năng gây nhiễm hay không. Do đó, nghiên cứu này với sự hỗ trợ của Phòng Thí nghiệm Bệnh học Nuôi trồng Thủy sản thuộc Đại học Arizona được thực hiện nhằm đánh giá khả năng lây nhiễm của WSSV trong tôm sau khi đã qua quá trình nấu chín.
Chuẩn bị nghiên cứu
Tôm trong nghiên cứu này đến từ một cơ sở nuôi tôm thương mại ở Hoa Kỳ. Tổng cộng 250 con tôm thẻ chân trắng (Litopenaeus vannamei) có chỉ số SPF và trọng lượng trung bình 10 gram đã được sử dụng. Trọng lượng mẫu này đại diện cho trọng lượng điển hình của tôm trong ao khi tiến hành thu hoạch khẩn cấp tại các trang trại nuôi tôm ở những nơi virus WSSV đang lưu hành và sắp xảy ra dịch bệnh.
Để tạo ra tôm nhiễm WSSV, một thử nghiệm gây nhiễm WSSV đã được tiến hành qua đường miệng bằng cách cho tôm L. vannamei không nhiễm WSSV (SPF) ăn mô tôm băm nhỏ đã được xác nhận nhiễm WSSV trước đó. Lượng thức ăn được chia thành 2 phần (sáng và tối) trong cùng một ngày, bằng 10% trọng lượng cơ thể của tôm SPF. Nước trong bể thí nghiệm được giữ ở độ mặn 25 ppt và nhiệt độ 25 độ C. Sau khi thử nghiệm gây nhiễm, tỷ lệ chết được đánh giá mỗi giờ. Tôm L. vannamei SPF được cho ăn mô tôm khỏe mạnh và được dùng làm nhóm đối chứng âm tính.
Khi tỷ lệ chết của tôm đạt 50%, những con sống sót được vớt ra để mô phỏng thu hoạch khẩn cấp và tiến hành giết mổ. Mẫu mang và chân bơi được thu thập và bảo quản để xác nhận bằng các xét nghiệm PCR thông thường và PCR thời gian thực. Năm con tôm có biểu hiện lâm sàng được cố định và bảo quản để phân tích mô học (Hình 1).
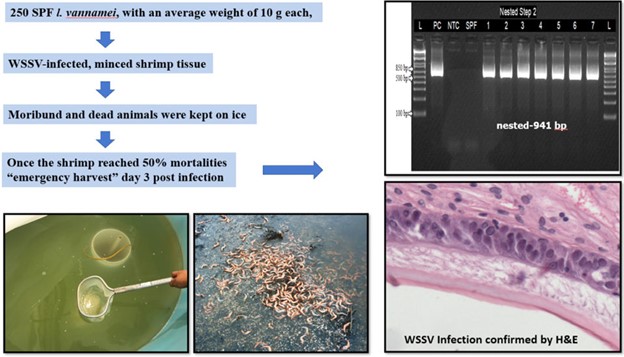
Quần thể tôm nhiễm bệnh ban đầu được chia thành sáu nhóm, mỗi nhóm gồm 40 cá thể, tương ứng với các thời gian xử lý bằng cách luộc trong nước ngọt là 0, 1, 3, 5, 10 và 30 phút. Một nhóm tôm không nhiễm WSSV được sử dụng làm đối chứng âm tính. Mỗi nhóm gồm 40 con tiếp tục được chia thành hai nhóm phụ, với hai lần lặp lại cho mỗi nhóm. Nhóm phụ thứ nhất được luộc theo các mốc thời gian quy định và sau đó dùng làm thức ăn cho tôm Litopenaeus vannamei khỏe mạnh. Nhóm phụ thứ hai cũng được xử lý nhiệt theo các mốc thời gian tương tự, nhưng được bảo quản đông ở –20°C trong 14 ngày trước khi cho tôm không nhiễm bệnh ăn (Hình 2).
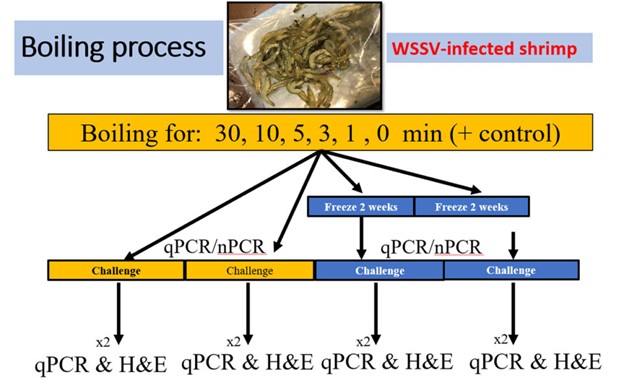
Nhiệt độ bên trong mô tôm được đo bằng nhiệt kế đặt trực tiếp trong phần cơ xương đuôi, và dữ liệu được ghi nhận trước cũng như sau quá trình nấu. Sau khi luộc, các mẫu được để nguội trong thời gian ngắn, sau đó mô mang và chân bơi được thu thập, bảo quản để phục vụ cho các phân tích tiếp theo bằng phương pháp PCR và qPCR (PCR định lượng – kỹ thuật cải tiến của PCR truyền thống, được sử dụng để phát hiện và định lượng axit nucleic trong nhiều lĩnh vực nghiên cứu).
Để đánh giá khả năng gây bệnh của tôm đã nấu chín, một thí nghiệm gây nhiễm được tiến hành trên quần thể tôm SPF. Mỗi bể thí nghiệm dung tích 90 lít được bố trí 10 con tôm giống, có khối lượng từ 2–3 g/con. Ở mỗi lần lặp và tại từng mốc thời gian, các mô gồm dạ dày, mang và chân bơi được thu thập từ toàn bộ tôm, sau đó cắt nhỏ và đưa vào bể theo hai đợt mỗi ngày (sáng và tối) với lượng tương đương 10% tổng khối lượng cơ thể của quần thể tôm SPF trong một ngày. Quá trình gây nhiễm kéo dài từ 11 đến 12 ngày. Tỷ lệ chết được ghi nhận hằng ngày, đồng thời các mẫu mang và chân bơi từ những cá thể sắp chết được thu thập và bảo quản để phát hiện virus WSSV bằng phương pháp qPCR và PCR. Ngoài ra, các cá thể sắp chết còn được cố định trong dung dịch Davidson nhằm phục vụ cho phân tích mô học.
Tỷ lệ sống tích lũy được ghi nhận tại thời điểm kết thúc quá trình thử thách. Mẫu chân bơi của toàn bộ tôm trong mỗi bể được thu thập và bảo quản trong dung dịch ethanol 95% để phục vụ phân tích PCR và qPCR. Đồng thời, hai cá thể tôm từ mỗi bể được cố định trong dung dịch Davidson nhằm thực hiện phân tích mô học.
Nhóm tôm được bảo quản đông lạnh trong vòng hai tuần (Nhóm 2) tiếp tục được sử dụng cho các thử nghiệm gây nhiễm WSSV theo quy trình tương tự như đã mô tả ở trên. Để biết thêm thông tin chi tiết về thiết kế thí nghiệm, phương pháp gây nhiễm, quy trình lấy mẫu và gộp mẫu, xử lý mẫu bằng đun sôi, thử nghiệm gây nhiễm WSSV, chiết xuất DNA, phân tích PCR/qPCR cũng như mô bệnh học, vui lòng liên hệ với tác giả liên hệ.
Kết quả
Mô tôm nhiễm WSSV được thêm vào bể thí nghiệm với mật độ tôm là 10,5 gram ± 1 gram đã gây ra tỷ lệ chết cao. Nhóm tôm đầu tiên bắt đầu chết vào ngày thứ 2 sau khi nhiễm bệnh (dpi). Vào ngày thứ 4 sau khi nhiễm bệnh, khi tỷ lệ chết đạt 50%, những con tôm sống sót đã được thu hoạch. Tôm được cố định bằng dung dịch Davidson đã được xác nhận dương tính với WSSV bằng PCR và H&E (nhuộm hematoxylin và eosin, hay nhuộm H&E, là một trong những phương pháp nhuộm mô chính được sử dụng trong mô học, nghiên cứu về giải phẫu vi mô của các mô sinh học; xem Hình 1). Ba mươi con tôm được thu thập trong quá trình thử nghiệm đã được giữ trên đá, sau đó được lấy mẫu và xác nhận dương tính với WSSV bằng qPCR và PCR lồng ghép (một biến thể của PCR được thiết kế để cải thiện tính đặc hiệu và độ nhạy).
Tôm nhiễm WSSV được xử lý ở các nhiệt độ luộc khác nhau (0, 1, 3, 5, 10 và 30 phút). Sau khi kết thúc quá trình luộc, mẫu mang và chân bơi được lấy để phân tích bằng PCR và qPCR. Bảng 1 tóm tắt kết quả qPCR và PCR lồng ghép đối với WSSV ở điều kiện không đông lạnh và đông lạnh trong hai tuần. Các mẫu thu thập sau khi luộc ở các thời gian khác nhau đều cho kết quả dương tính với WSSV bằng qPCR. Ngược lại, không có mẫu nào cho kết quả khuếch đại bằng PCR lồng ghép.
Bảng 1a. Tóm tắt kết quả qPCR và nested PCR thu được bằng cách sử dụng DNA phân lập từ các mẫu tôm được xử lý ở các thời gian luộc khác nhau.
| Mô tả bể chứa (không tính thời gian đóng băng) | qPCR WSSV – Số ca dương tính/Tổng số ca | Giá trị Ct – Trung bình ± Độ lệch chuẩn | Xét nghiệm PCR lồng ghép WSSV – Số mẫu dương tính/Tổng số mẫu |
| Đối chứng âm tính | 0/4 | Không phát hiện | ND (0/1) |
| WSSV nấu trong 30 phút | 4/4 | 21,48±3,05 | ND (0/1) |
| WSSV nấu trong 10 phút | 4/4 | 18,44 ± 0,61 | ND (0/1) |
| WSSV nấu trong 5 phút | 4/4 | 20,54 ±3,20 | ND (0/1) |
| WSSV nấu trong 3 phút | 4/4 | 20,01 ± 1,81 | ND (0/1) |
| WSSV nấu trong 1 phút | 4/4 | 25,73 ± 5,00 | ND (0/1) |
| WSSV nấu trong 0 phút (Đối chứng dương) | 4/4 | 20,35 ± 2,50 | Dương tính (1/1) |
Bảng 1b. Tóm tắt kết quả qPCR và nested PCR thu được bằng cách sử dụng DNA phân lập từ mẫu tôm được xử lý ở các thời gian luộc khác nhau.
| Mô tả bể chứa (đóng băng trong 2 tuần) | qPCR WSSV – Số ca dương tính/Tổng số ca | Giá trị Ct – Trung bình ± Độ lệch chuẩn | Xét nghiệm PCR lồng ghép WSSV – Số mẫu dương tính/Tổng số mẫu |
| Kiểm soát âm tính | 0/4 | Không phát hiện | ND (0/1) |
| WSSV nấu trong 30 phút | 4/4 | 21,10±2,29 | ND (0/1) |
| WSSV nấu trong 10 phút | 4/4 | 21,22±1,30 | ND (0/1) |
| WSSV nấu trong 5 phút | 4/4 | 22,99±2,15 | ND (0/1) |
| WSSV nấu trong 3 phút | 4/4 | 22,16±2,06 | ND (0/1) |
| WSSV nấu trong 1 phút | 4/4 | 20,65±1,03 | ND (0/1) |
| WSSV nấu trong 0 phút (Đối chứng dương) | 4/4 | 21,34±2,63 | Dương tính (1/1) |
Trong nghiệm thức 1, mô tôm bị nhiễm WSSV và được xử lý ở các thời gian luộc khác nhau được sử dụng làm chất gây nhiễm trong thử nghiệm cảm nhiễm qua đường miệng sử dụng tôm L. vannamei SPF . Bảng 2 tóm tắt tỷ lệ sống của tôm sau 10 ngày sau khi nhiễm bệnh.
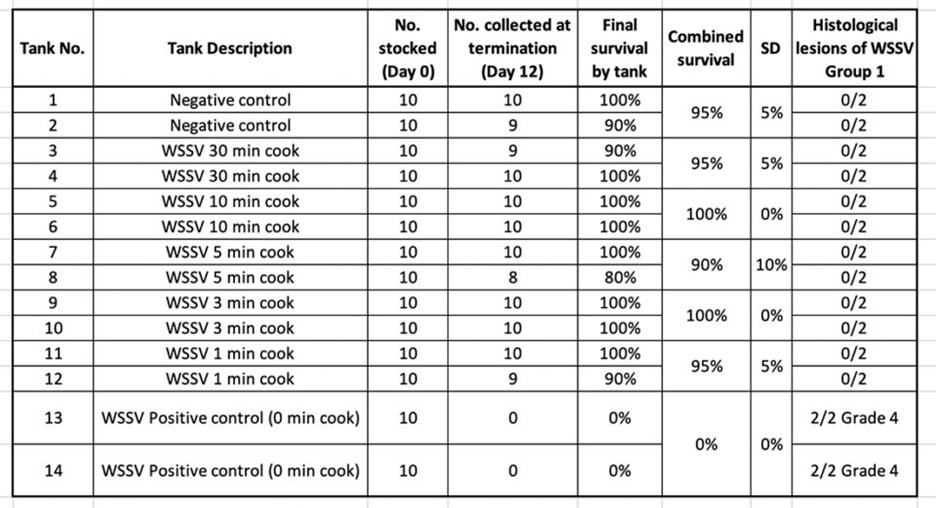
Tỷ lệ chết cao chỉ được ghi nhận ở các bể đối chứng dương tính với WSSV, trong đó tôm được xử lý nhiệt trong thời gian 0 phút. Kết quả nhuộm H&E và phân tích PCR đã xác nhận sự hiện diện của WSSV trong các bể này. Hiện tượng tương tự cũng được quan sát khi tôm luộc được bảo quản đông lạnh trong hai tuần và sau đó sử dụng làm nguồn vật liệu gây nhiễm.
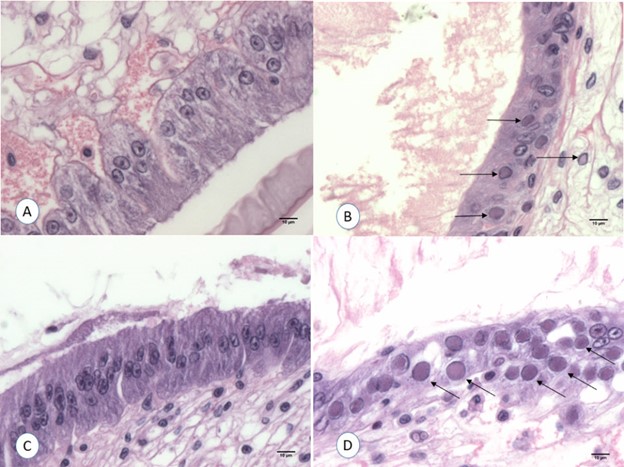
Các mẫu mô thu thập từ các nghiệm thức khác nhau vào cuối thí nghiệm đã được phân tích bằng phương pháp nhuộm H&E. Kết quả cho thấy sự xuất hiện của các thể vùi ưa bazơ nội nhân đặc trưng của WSSV trong các nhân tế bào bị phì đại, chủ yếu tại một số mô có nguồn gốc từ ngoại bì và trung bì. Hình 3 minh họa các tổn thương mô học điển hình của WSSV ở mức độ 4.0 trong biểu mô lớp biểu bì dạ dày của bể đối chứng dương tính. Ngược lại, ở các nhóm tôm được cho ăn mô tôm đã luộc trong các khoảng thời gian khác nhau (1, 3, 5, 10 và 30 phút), không ghi nhận bất kỳ tổn thương mô học đặc trưng nào của WSSV.
Các mẫu của cá thể non được gây nhiễm thử nghiệm bằng tôm luộc và cho kết quả dương tính với WSSV bằng phương pháp qPCR đều cho kết quả âm tính trong tất cả các trường hợp (Bảng 3).
Bảng 3. Tóm tắt kết quả qPCR ở tôm SPF bị nhiễm WSSV và tiếp xúc với tôm đã luộc ở các thời gian khác nhau.
| Ao thi nghiệm | Tôm nhiễm WSSV được nấu ở các thời điểm khác nhau. | qPCR WSSV – Số ca dương tính/Tổng số ca | Giá trị Ct – Trung bình ± Độ lệch chuẩn |
| Thử thách tôm SPF với tôm SPF | Kiểm soát âm tính | 0/4 | ND |
| Thử nghiệm tôm SPF với tôm nhiễm WSSV được nấu trong 30 phút. | Thử thách SPF với tôm nấu trong 30 phút theo phương pháp WSSV. | 0/4 | ND |
| Thử nghiệm tôm SPF với tôm nhiễm WSSV được nấu trong 10 phút. | WSSV nấu trong 10 phút | 0/4 | ND |
| Thử nghiệm tôm SPF với tôm nhiễm WSSV được nấu trong 5 phút. | WSSV nấu trong 5 phút | 0/4 | ND |
| Thử nghiệm tôm SPF với tôm nhiễm WSSV được nấu trong 3 phút. | WSSV nấu trong 3 phút | 0/4 | ND |
| Thử nghiệm tôm SPF với tôm nhiễm WSSV được nấu trong 1 phút. | WSSV nấu trong 1 phút | 0/4 | ND |
| Thử nghiệm tôm SPF với tôm nhiễm WSSV được nấu trong 0 phút | Mẫu đối chứng dương WSSV (thời gian nấu 0 phút) | 4/4 | 21,57±1,73 |
Thảo luận
Kết quả nghiên cứu cho thấy tôm nhiễm WSSV sau khi tiếp xúc với nhiệt độ sôi trong khoảng từ 1 đến 30 phút đã hoàn toàn mất khả năng lây nhiễm. Phân tích bằng phương pháp qPCR xác nhận sự hiện diện của DNA WSSV trong tất cả các mẫu được đun sôi ở các khoảng thời gian khác nhau, đồng thời không ghi nhận sự khác biệt đáng kể về giá trị Ct giữa các nghiệm thức (P < 0,05). Tuy nhiên, không có mẫu nào cho kết quả khuếch đại thành công khi sử dụng phương pháp PCR lồng ghép để phát hiện WSSV.
Mặc dù qPCR cho kết quả dương tính, trái ngược với kết quả âm tính của PCR lồng ghép, nhưng điều này nhiều khả năng xuất phát từ việc DNA WSSV phân lập từ tôm đã qua xử lý nhiệt bị tổn hại nghiêm trọng, dẫn đến chất lượng suy giảm và mức độ phân mảnh cao hơn so với DNA từ mẫu tôm tươi. Trong phương pháp PCR lồng ghép, kích thước dự kiến của đoạn khuếch đại ở bước thứ nhất là 1.447 bp, và đoạn khuếch đại nội ở bước thứ hai là 941 bp. Việc không phát hiện được các đoạn khuếch đại này cho thấy DNA WSSV đã bị phân hủy thành các đoạn nhỏ hơn, từ đó làm mất khả năng lây nhiễm của virus. Ngược lại, kích thước đoạn khuếch đại trong qPCR chỉ khoảng 69 bp, nhỏ hơn đáng kể so với PCR lồng ghép. Do đó, ngay cả khi DNA WSSV bị phân mảnh trong quá trình đun sôi, các đoạn ngắn này vẫn có thể được khuếch đại, dẫn đến kết quả dương tính khi phân tích bằng qPCR.
Nhằm xác minh khả năng lây nhiễm của tôm L. vannamei nhiễm WSSV chỉ cho kết quả dương tính qua qPCR, một thí nghiệm gây nhiễm thực nghiệm trên tôm SPF đã được tiến hành. Kết quả cho thấy, tỷ lệ sống cuối cùng ở tất cả các bể thí nghiệm đều cao khi tôm được cho ăn mô băm nhỏ dương tính với WSSV và đã được đun sôi trong khoảng thời gian từ 1 đến 30 phút. Ngược lại, hiện tượng tử vong chỉ ghi nhận ở nhóm tôm tiếp xúc với mô dương tính đối chứng chưa qua xử lý nhiệt (đun sôi 0 phút). Sau khi kết thúc thí nghiệm, tôm sống sót từ tất cả các bể được phân tích bằng phương pháp nhuộm H&E và qPCR. Các thể vùi đặc trưng của WSSV trong biểu mô và mô liên kết chỉ được phát hiện ở nhóm tôm sử dụng mô đối chứng dương tính. Trong khi đó, các mẫu mô của tôm được gây nhiễm bằng mô dương tính với WSSV đã đun sôi trong 1, 3, 5, 10 và 30 phút không xuất hiện bất kỳ tổn thương mô học đặc trưng nào của nhiễm WSSV. Hình 3A và 3C minh họa mặt cắt mô học dạ dày của tôm tiếp xúc với mô dương tính được đun sôi trong 1 phút. Phân tích qPCR trên hai mẫu gộp từ mỗi bể chỉ ghi nhận kết quả dương tính ở nhóm đối chứng dương tính.
Những kết quả này cho thấy việc xử lý nhiệt thông qua nấu chín có thể làm giảm nguy cơ lây lan WSSV trong chuỗi xuất nhập khẩu tôm nuôi trên phạm vi toàn cầu. Đồng thời, phương pháp này cũng có tiềm năng được ứng dụng để kiểm tra và kiểm soát các mầm bệnh khác gây hại cho tôm nuôi, bao gồm virus, vi khuẩn và nấm.
Kết luận
Trong nghiên cứu này, tôm nhiễm WSSV được luộc ở nhiệt độ sôi trong các khoảng thời gian khác nhau, bao gồm 0, 1, 3, 5, 10 và 30 phút. Sau quá trình xử lý nhiệt, các mẫu tôm được sử dụng làm thức ăn cho tôm thẻ chân trắng (Litopenaeus vannamei) nhằm đánh giá khả năng lây nhiễm.
Kết quả cho thấy nhóm đối chứng dương (0 phút) vẫn gây nhiễm WSSV cho tôm thử nghiệm. Ngược lại, các nhóm được xử lý nhiệt trong 1, 3, 5, 10 và 30 phút không ghi nhận hiện tượng nhiễm WSSV. Phân tích tỷ lệ chết cho thấy chỉ nhóm đối chứng dương có mức chết cao, trong khi không ghi nhận trường hợp chết ở các nhóm còn lại. Những kết quả này cho thấy việc luộc tôm ở nhiệt độ sôi trong ít nhất 1 phút có thể làm bất hoạt WSSV và hạn chế nguy cơ lây lan mầm bệnh từ các khu vực lưu hành sang những vùng chưa ghi nhận sự hiện diện của virus. Ngoài ra, nghiên cứu khuyến nghị sử dụng phương pháp lồng ghép sinh học để đánh giá khả năng lây nhiễm của tôm đã qua xử lý nhiệt, thay vì chỉ dựa trên phương pháp qPCR.
Theo Luis Fernando Aranguren Caro, Hung N. Mai, Linda Nunan, Joshua Lin, Brenda Noble, Arun K. Dhar
Biên dịch: Nguyễn Thị Quyên – Tôm Giống Gia Hóa Bình Minh
Xem thêm:
- Phần 1: Chiết Xuất Bã Tinh Dầu Của Cây Tía Tô Có Hoạt Tính Sinh Học, Dùng Làm Chất Chống Oxy Hóa Và Chất Bảo Quản Chống Đen Cho Tôm Thẻ Chân Trắng
- Phần 2: Chiết Xuất Bã Tinh Dầu Của Cây Tía Tô Có Hoạt Tính Sinh Học, Dùng Làm Chất Chống Oxy Hóa Và Chất Bảo Quản Chống Đen Cho Tôm Thẻ Chân Trắng
- Phân Tích Bệnh Phân Trắng (WFD) do Vibrio sp. Và Dinoflagellata Ở Tôm Thẻ Chân Trắng (Litopenaeus vannamei) Ở Ao Nuôi Nước Lợ

 English
English 中文 (中国)
中文 (中国)
SẢN PHẨM PHỤC VỤ NỀN NÔNG NGHIỆP XANH
TIN TỨC NỔI BẬT
Nồng Độ Nitrat Cao Gây Độc Cho Tôm
Độc tính là vấn đề nghiêm trọng hơn ở những vùng nước có độ mặn [...]
Th6
Mùi Vị Lạ Trong Các Sản Phẩm Nuôi Trồng Thủy Sản, Phần 3
Ảnh hưởng của thức ăn chăn nuôi, quá trình chế biến và bảo quản. Xu [...]
Th6
Mùi Vị Lạ Trong Các Sản Phẩm Nuôi Trồng Thủy Sản, Phần 2
Nước sử dụng trong nuôi trồng thủy sản có thể bị ảnh hưởng bởi các [...]
Th6
Mùi Vị Lạ Trong Các Sản Phẩm Nuôi Trồng Thủy Sản, Phần 1
Geosmin, 2-Methylisoborneol Đặc tính cảm quan của cá và các loài động vật có vỏ [...]
Th5
Nuôi Cá Rô Phi Lai Trong Hệ Thống Sản Xuất Sinh Học Ngoài Trời
Hàm lượng protein dễ tiêu hóa có thể được giảm bớt mà không ảnh hưởng [...]
Th5
Cá Rô Phi: Khám Phá Nguồn Gốc Và Môi Trường Sống
Cá rô phi được xem là biểu trưng cho khả năng thích nghi , khoẻ [...]
Th5
Các Biện Pháp Xử Lý Sau Thu Hoạch Tiêu Diệt Vi Khuẩn Vibrio vulnificus
Vi khuẩn chiếm 95% tổng số ca tử vong liên quan đến hải sản ở [...]
Th5
Tôm Thẻ Đối Kháng EMS, EHP, TPD – Bình Minh Ra Mắt Dòng Tôm Thẻ Gia Hóa Thế Hệ Mới
Trong những năm gần đây, người nuôi tôm tại Việt Nam liên tục đối mặt [...]
Th5
Ưu Điểm Vượt Trội Của Cá Rô Phi Đơn Tính: Vì Sao Nên Chọn Nuôi?
Cá rô phi đơn tính (toàn đực) ngày càng được ưa chuộng trong ngành nuôi [...]
Th5
Sự Phân Hủy Hạn Chế Giúp Tăng Cường Khả Năng Phát Hiện Vibrio AHPND Trong Tôm Bằng Phương Pháp PCR
Xét nghiệm PCR có thể được sử dụng để phân biệt các chủng gây bệnh [...]
Th5
Cà Mau: Hộ Nuôi Tôm Vượt Qua EMS, EHP Nhờ Thay Đổi Quy Trình Và Chọn Đúng Con Giống
Trong khoảng 5 năm trở lại đây, EMS và EHP đã trở thành nỗi lo [...]
Th5
Artemia, “Bột Thần Kỳ” Thúc Đẩy Một Ngành Công Nghiệp Trị Giá Hàng Tỷ Đô La
Các trại sản xuất giống hiện vẫn phụ thuộc vào Artemia – nguồn thức ăn [...]
Th5