Tóm tắt
Enterocytozoon hepatopenaei (EHP), vi bào tử trùng, được xem là một mối đe dọa lớn đối với ngành nuôi tôm trong những năm gần đây. Cơ quan chủ đích mà vi bào tử trùng này nhắm đến là gan tụy tôm (HP); do đó, bệnh do EHP gây ra được gọi là bệnh nhiễm vi bào tử trùng (HPM). Gan tụy (HP) là tuyến tiêu hóa quan trọng nhất chịu trách nhiệm bài tiết, tiêu hóa, hấp thụ, dự trữ và chuyển hóa. Trong nghiên cứu này, tôm nhiễm EHP được nuôi đến 90 ngày và được kiểm tra về các phản ứng tiêu hóa, sinh lý, miễn dịch và tăng trưởng ở các khoảng thời gian khác nhau và so với tôm đối chứng. Kết quả kiểm tra mô học cho thấy các tế bào biểu mô và ống HP bị hoại tử nghiêm trọng, các giai đoạn phát triển của EHP, và các bào tử EHP trưởng thành trong tế bào chất biểu mô và lòng ống HP ở nhóm tôm cảm nhiễm. Các enzym tiêu hóa α-amylase và lipase đã giảm đáng kể (P <0,05) trong nhóm được cảm nhiễm EHP. Các chỉ số chuyển hóa như triglycerid (TG), tổng số protein (TP), cholesterol (CL), glucose (GL) và alanin aminotransferase (ALT) thấp đáng kể (P <0,05) ở nhóm cảm nhiễm EHP. Nhiễm EHP (P <0,05) gây ảnh hưởng đến phản ứng miễn dịch không đặc hiệu thông qua việc giảm hoạt động của alkaline phosphatase (ALP), catalase (CAT), γ- glutamyl transferase (GGT), tổng khả năng chống oxy hóa (T-AOC), anion superoxide (SOA), phenoloxidase (PO) và tổng số lượng hemocyte (THC). Sau 90 ngày, tăng trưởng của tôm ở nhóm cảm nhiễm EHP là 12,17 ± 0,80 g, trong khi nhóm đối chứng là 19,27 ± 0,5 g. Trọng lượng trung bình hàng ngày của nhóm cảm nhiễm là 96,72 ± 10,2 mg, và đối chứng là 175,34 ± 5,9 mg. FCR của nhóm cảm nhiễm là 3,01 ± 0,29, trong khi nhóm đối chứng là 1,64 ± 0,05. Tuy nhiên, tỷ lệ tôm sống sót sau khi nhiễm EHP sau 90 ngày là 71,1%. Do đó, tổn thương nghiêm trọng do EHP gây ra ở HP đã ảnh hưởng đến quá trình bài tiết, tiêu hóa, hấp thụ và dự trữ. Những tác động này ảnh hưởng đến sinh lý, chuyển hóa lipid, chuyển hóa carbohydrate, hệ thống miễn dịch và làm giảm khả năng tiêu thụ thức ăn, tăng FCR và chậm lớn. Kết luận, nhiễm EHP không gây chết hàng loạt nhưng làm chậm đáng kể tốc độ tăng trưởng của tôm, do đó làm tăng chi phí sản xuất và dẫn đến thiệt hại kinh tế nặng nề ở các trang trại nuôi tôm.
1/ Giới thiệu
Vi bào tử trùng là ký sinh trùng nội bào bắt buộc hình thành bào tử, được báo cáo ở động vật có xương sống, động vật không xương sống và một số sinh vật nguyên sinh. Chúng hiện diện ở khắp nơi và sự phân bố của chúng được báo cáo rộng rãi trong môi trường nước ngọt, nước lợ và nước mặn. Gần đây, Enterocytozoon hepatopaenaei (EHP), một vi bào tử trùng gây bệnh nhiễm khuẩn gan tụy (HPM), đã được báo cáo là ảnh hưởng đáng kể đến việc nuôi tôm và gây thiệt hại nghiệm trọng về kinh tế cho các quốc gia nuôi tôm. Tổn thất về mặt sản lượng do nhiễm EHP tại các trang trại nuôi tôm ở Ấn Độ được báo cáo là 0,77 triệu tấn, với mức thiệt hại về doanh thu lên đến 567,62 triệu đô la Mỹ (Patil và cộng sự, 2021).
Nhiễm EHP không gây chết hàng loạt nhưng chúng có khả năng liên quan đến sự chậm lớn và thay đổi kích thước (Biju và cộng sự, 2016; Chaijarasphong và cộng sự, 2020; Geetha và cộng sự, 2022; Ning và cộng sự, 2021; Rajendran và cộng sự, 2016). Có rất ít nghiên cứu liên quan đến EHP về sự chậm lớn của tôm (Chaijarasphong và cộng sự, 2020; Shen và cộng sự, 2021). Ngoài ra, một số nghiên cứu về phiên mã và protein đã điều tra sự chuyển hóa năng lượng, tăng trưởng và biểu hiện protein / gen miễn dịch liên quan đến nhiễm EHP (Duan và cộng sự, 2021; Ning và cộng sự, 2019; Yang và cộng sự, 2021). Gan tụy là cơ quan đóng vai trò chính trong việc tiết enzym tiêu hóa, tiêu hóa thức ăn, hấp thụ và dự trữ lipid, glycogen và khoáng chất (Wang và cộng sự, 2014). Cơ quan chủ đích mà EHP nhắm đến là gan tụy. Sự nhiễm trùng trên gan tụy có thể ảnh hưởng đến sự bài tiết men tiêu hóa, tiêu hóa, hấp thụ và chuyển hóa chất dinh dưỡng. Các biến số chuyển hóa, như triglyceride (TG), tổng số protein (TP), cholesterol (CL), glucose (GLU), alanine aminotransferase (ALT) và aspartate aminotransferase (AST) được sử dụng làm chỉ số về tình trạng sinh lý của tôm (Mercier và cộng sự, 2006; Rosas và cộng sự, 2004). Tổng số lượng hemocyte (THC), propnoloxidase (PO), superoxide anion (SOA), superoxide dismutase (SOD), tổng lượng antioxidants (T-AOC) và catalase (CAT) được sử dụng làm chỉ số về tình trạng miễn dịch của tôm (Rosas và cộng sự, 2004).
Trong nghiên cứu này, ảnh hưởng và mối liên quan của EHP đối với tăng trưởng của tôm được điều tra tổng thể bằng cách phân tích các enzym tiêu hóa (α-amylase, lipase), phản ứng chuyển hóa (triglyceride (TG), tổng số protein (TP), glucose (GLU), cholesterol (CL), alanine aminotransferase (ALT), aspartase aminotransferase (AST)), phản ứng miễn dịch (tổng số lượng hemocyte (THC), alkaline phosphatase (ALP), γ- glutamyl transferase (GGT), superoxide anion (SOA), catalase (CAT), propnoloxidase (PO), tổng khả năng chống oxy hóa (T-AOC)) và hiệu suất tăng trưởng của tôm P. vannamei bị nhiễm EHP trong thử nghiệm.
2/ Vật liệu và phương pháp
2.1. Thiết kế thử nghiệm
Tôm thẻ P. vannamei giai đoạn juveniles (tôm chưa trưởng thành) (4 g ± 0,21 g) được lấy từ trung tâm Nghiên cứu Muttukadu của ICAR-Viện Trung ương Nuôi trồng Thủy sản Nước lợ, Tamil Nadu, Ấn Độ. Trước khi bắt đầu thử nghiệm, tôm được xét nghiệm PCR để kiểm tra WSSV (Kimura và cộng sự, 1996), IHHNV (OIE, 2019), IMNV (OIE, 2019) và EHP (Jaroenlak và cộng sự, 2016). Tôm âm tính với WSSV, IHHNV, IMNV và EHP sẽ được sử dụng cho thí nghiệm. Nhóm thử nghiệm (n = 30) có mô HP dương tính với EHP (106 bản sao EHP / ng DNA) (Sathish Kumar và cộng sự, 2022) được cho ăn lặp lại 3 lần bằng thức ăn viên nhân tạo cỡ nhỏ trong 3 ngày cho đến khi có dấu hiệu no rõ ràng. Nhóm đối chứng (n = 30) có mô HP âm tính với EHP, cũng với 3 lần lặp lại, được cho ăn bằng thức ăn cho tôm cho đến khi có dấu hiệu no rõ ràng. Thí nghiệm được thực hiện trong điều kiện phòng thí nghiệm có kiểm soát (độ mặn 27 ppt, nhiệt độ 29°C, pH 7,9 ± 0,3) trong bể hình tròn 200L trong 90 ngày. Để đánh giá sự tăng trưởng và khả năng sống sót, tôm được lấy mẫu định kỳ hàng tuần. Theo đó, dựa trên sinh khối, tỷ lệ cho ăn đã được điều chỉnh để đạt được độ no rõ ràng trong quá trình thử nghiệm. Đối với các nghiên cứu về enzyme, mô học, mẫu (gan tụy và hemolymph) (n = 3) cho mỗi lần lặp lại được thu thập sau ngày cảm nhiễm thứ 15, 30, 60 và 90. Đối với PCR, các mẫu được thu thập sau ngày cảm nhiễm thứ 7, 15, 30, 60 và 90.
2.2. Kính hiển vi ánh sáng và mô học
Mẫu phết trên lam kính được lấy từ gan tụy và các sợi phân của cả nhóm thử nghiệm và nhóm đối chứng đã được quan sát dưới kính hiển vi. Gan tụy tôm được thu thập vào các khoảng thời gian khác nhau và được cố định trong dung dịch Davidson (Bell và Lightner, 1988) và xử lý mô học, nhuộm bằng H&E. Ngoài ra, các phần mô và mẫu phết trên lam kính được nhuộm bằng CFW (Zhao và cộng sự, 2020) và được quan sát dưới kính hiển vi ánh sáng.
2.3. Kính hiển vi điện tử quét và kính hiển vi điện tử truyền qua
Đối với kính hiển vi điện tử truyền qua, mô HP được cố định trong 2,5% glutaraldehyde trong dung dịch đệm sodium cacodylate 0,1 M (pH 7,4) trong 8 giờ ở 4°C và được cố định bằng 1% osmium tetroxide trong dung dịch đệm sodium cacodylate 0,1 M (pH 7,4) và được xử lý như đã mô tả trước đó (Sathish Kumar và cộng sự, 2017). Sau đó, các mẫu được quan sát bằng kính hiển vi điện tử truyền qua (TEM) JEM 1400 (JEOL Ltd., Nhật Bản) tại Viện Nghiên cứu Ung thư (WIA), Chennai.
Đối với kính hiển vi điện tử quét, các mẫu phân được cố định trong dung dịch đệm glutaraldehyde 2,5% (Sigma Aldrich, Hoa Kỳ) trong 8 giờ ở 4°C và được khử nước bằng etanol và HMDS như đã mô tả (Nikara và cộng sự, 2020). Các mẫu được xem bằng kính hiển vi điện tử quét JSM IT 300LV (JEOL Ltd., Nhật Bản) (SEM) tại ICAR-Viện Trung ương Nuôi trồng Thủy sản Nước lợ, Chennai.
2.4. Tách chiết DNA, xét nghiệm PCR và qPCR
Để tách chiết DNA, gan tụy và phân được thu thập từ cả nhóm thử nghiệm và nhóm đối chứng và đồng nhất ở 4°C. Tổng số DNA được chiết xuất từ 100 μl của các mẫu được đồng nhất bằng cách phân giải với 500 μl dung dịch đệm CTAB theo các quy trình được đưa ra trước đó (Sathish Kumar và cộng sự, 2022). Quá trình khuếch đại PCR được thực hiện trong phản ứng 25 μl bằng cách sử dụng mồi SWP-PCR (Jaroenlak và cộng sự, 2016). Các sản phẩm khuếch đại được phân giải trên gel agarose 1,8%. Xét nghiệm qPCR được thực hiện với 20 μl hỗn hợp đệm bao gồm Premix Ex Taq (mẫu dò qPCR) (Takara, Nhật Bản) một enzyme PCR khởi động nóng kết hợp với kháng thể kháng Taq hiệu suất cao, 0,25 μM mỗi mồi thuận và nghịch và 0,125 μM mẫu dò TaqMan như đã báo cáo trước đó (Sathish Kumar và cộng sự, 2022). Plasmid chứa amplicon đích đã được pha loãng theo trình tự và được sử dụng làm chất chuẩn trong phân tích qPCR.
2.5. Thu thập và phân tích mẫu hemocyte
Hemolymph được thu thập từ xoang bụng bằng cách sử dụng ống tiêm vô trùng 1 ml 26 vạch có dung dịch đệm chống đông máu (30 mM tri‑sodium citrate, 388 mM NaCl, 0,12 M glucose, 10 mM EDTA, pH 7,8) theo tỷ lệ 1:10 (hemolymph: chất chống đông máu) để ước tính tổng số lượng hemocyte (THC). THC được thống kê thủ công bằng cách sử dụng máy đo hemocyte (Kumar và cộng sự, 2015). Đối với các nghiên cứu về enzyme, hemolymph được thu thập mà không cần chất đệm chống đông máu, được làm đông 30 phút trong nước đá, và được xử lý để phân tích.
2.6. Phân tích enzyme tiêu hóa, sinh hóa và miễn dịch
100 mg HP và 100 μl hemolymph được thu thập và đồng nhất với 900 μl 1 × PBS và được xử lý để phân tích sinh hóa và enzyme. α- amylase (phương pháp cơ chất trực tiếp), lipase (Phương pháp đo độ đục U.V.), chất béo trung tính (TG) (Phương pháp GPO / PAP), Glucose (GLU) (Phương pháp GOD / POD), cholesterol (CL) (Phương pháp CHOD / PAP), tổng số protein (TP) (Phương pháp Biuret), aspartate aminotransferase (AST) (Phương pháp IFCC Mod), alanine aminotransferase (ALT) (Phương pháp IFCC Mod), alkaline phosphatase (ALP) (Phương pháp Mod. của Kind & King) và giá trị γ- glutamyl transferase (GGT) (CarboXy Substrate Method) được ước tính bằng cách sử dụng bộ dụng cụ thương mại theo hướng dẫn của nhà sản xuất (Coral Clinical Systems, Goa, India). Hoạt động của enzyme miễn dịch superoxide anion, tổng chất chống oxy hóa (T-AOC), catalase (CAT) được tính toán bằng cách sử dụng các bộ công cụ thương mại theo quy trình của nhà sản xuất (Origin, Kerala, India). Hoạt động của phenoloxidase (PO) được đo bằng cách làm theo quy trình được mô tả bởi Panigrahi và cộng sự (2020). Đối với hemolymph, tăng gấp đôi tỷ lệ trypsin cần thêm vào và tạo thành 200 μl với 5 mM L-DOPA. Hỗn hợp này được ủ trong 20 phút ở 25°C, và giá trị OD được đo ở bước sóng 490 nm sử dụng đầu đọc vi tấm đa chức năng Spark ™ 10 M (TECAN, Thụy Sĩ) để ước tính hoạt tính của enzyme.
2.7. Hiệu suất tăng trưởng
Trọng lượng cơ thể của tôm trong nhóm đối chứng và nhóm thử nghiệm được đo cách nhau hàng tuần. Tăng trưởng, lượng thức ăn tiêu thụ và tỷ lệ sống của tôm được đánh giá bằng các thông số như trọng lượng cơ thể trung bình, tăng trọng (WG), hệ số chuyển đổi thức ăn (FCR), tăng trưởng trung bình hàng ngày (ADG), chỉ số gan (HSI) và tỷ lệ sống (Panigrahi và cộng sự, 2019). Sản lượng dự kiến trên một ha (t/ha) được ước tính bằng cách sử dụng các thông số như mật độ thả (40 con/m2), trọng lượng cơ thể trung bình cuối cùng và tỷ lệ sống (%).
2.8. Phân tích thống kê
Phân tích thống kê được thực hiện bằng phần mềm SPSS v 16.0. Phân tích phương sai một chiều (ANOVA) và phép kiểm t-student được sử dụng để ước tính ý nghĩa thống kê ở P <0,05. Dữ liệu số được trình bày trong tất cả các hình và bảng là giá trị trung bình ± độ lệch chuẩn (SD).
3/ Kết quả
3.1. Kính hiển vi ánh sáng và mô học
Mẫu phết HP và sợi phân đã cảm nhiễm EHP được nhuộm bằng CFW rõ ràng cho thấy sự hiện diện dày đặc của các bào tử EHP trưởng thành trong mọi khoảng thời gian. Kiểm tra mô học gan tụy của nhóm cảm nhiễm cho thấy sự hoại tử của các tế bào biểu mô, sự tách rời của các tế bào biểu mô khỏi màng đáy, các ống HP bị giãn, hình thành trong xoang máu, thâm nhiễm hemocyte, sự đóng gói và bong tróc của các tế bào biểu mô, các giai đoạn phát triển của EHP, bao gồm các thể ưa bazơ trong tế bào chất của tế bào biểu mô, các cấu trúc giống plasmodial xung quanh các tế bào biểu mô bong tróc, và sự hiện diện của các bào tử trưởng thành và các khối bào tử khối trong tế bào chất và lòng ống của tế bào biểu mô. Trong tất cả các khoảng thời gian, sự hoại tử tương đối nghiêm trọng của các ống HP được quan sát thấy sau ngày cảm nhiễm thứ 30 (Hình 1).
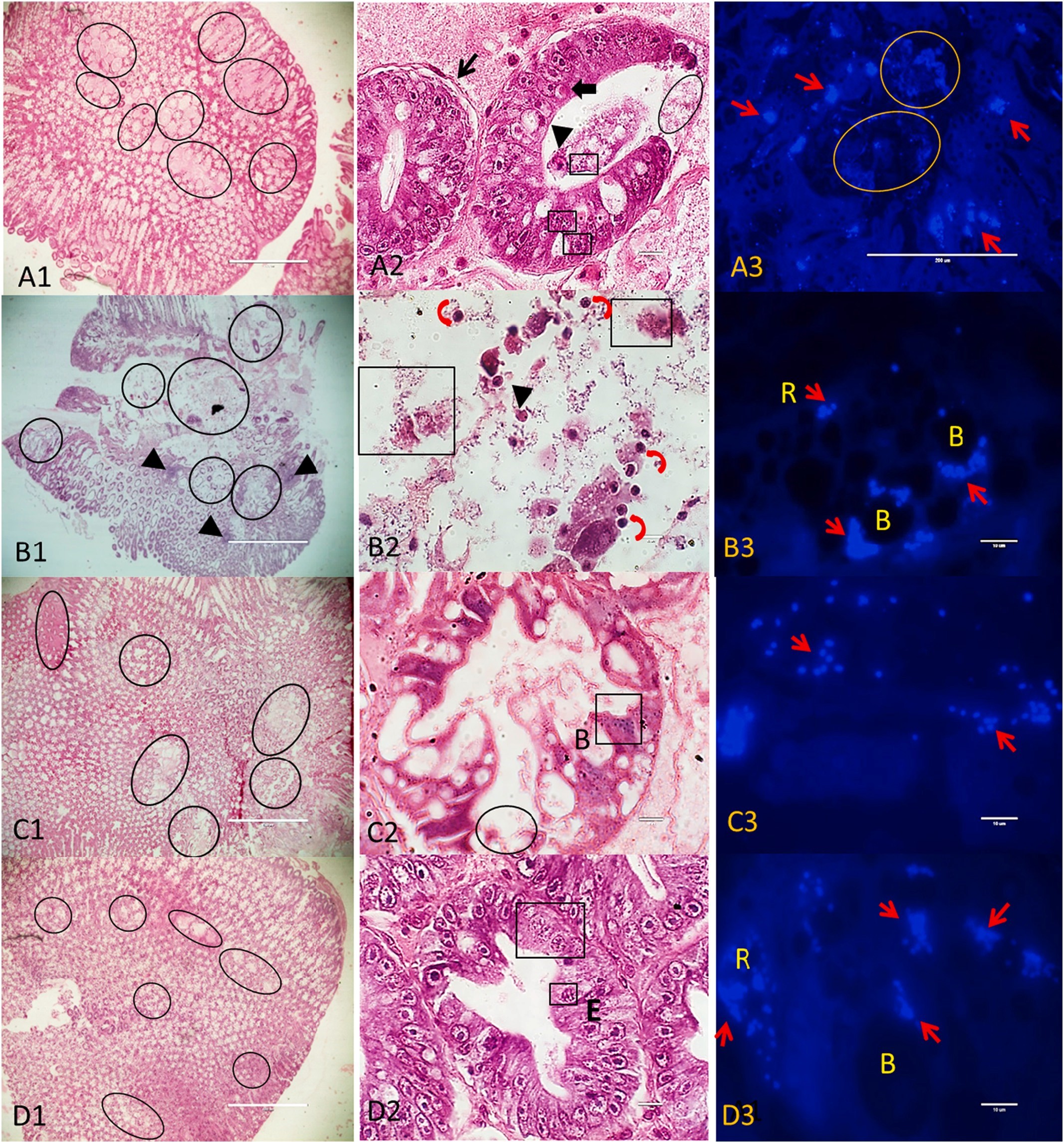
Hình 1. HP tôm sau ngày cảm nhiễm thứ 15 (A), 30 (B), 60 (C), 90 (D). A1, B1, C1, D1 – biểu hiện hoại tử nghiêm trọng của ống HP (hình tròn), đóng gói tế bào máu (đầu mũi tên), A2, B2, C2, D2 – bào tử trưởng thành (hình vuông), sự tách rời của biểu mô ống HP khỏi màng đáy (mũi tên), bao gồm ưa acid như giai đoạn plasmodial đầu (mũi tên khối), giai đoạn plasmodial cuối (mũi tên cong), tế bào biểu mô bong tróc (đầu mũi tên), hoại tử nặng (vòng tròn), A3, B3, C3, D3- bào tử trưởng thành và khối bào tử (mũi tên) trong tế bào chất biểu mô, tế bào biểu mô bị hoại tử nặng (hình tròn), tế bào B- B, tế bào R- R, tế bào E- E.
3.2. Kính hiển vi điện tử truyền qua và kính hiển vi quét
TEM của HP được cảm nhiễm với EHP cho thấy sự co thắt túi bào tử và bào tử trưởng thành trong tế bào chất của tế bào biểu mô thường được bao quanh bởi ty thể vật chủ (Hình 2A). SEM của các chuỗi phân được cảm nhiễm với EHP cho thấy sự hiện diện của các bào tử trưởng thành, dày đặc ở mọi khoảng thời gian (Hình 2B).

Hình 2. Hình A- TEM của HP đã cảm nhiễm EHP cho thấy các bào tử trưởng thành trong tế bào chất biểu mô được bao quanh bởi ty thể vật chủ. Hình B- SEM của phân đã cảm nhiễm EHP cho thấy các bào tử trưởng thành. S- Bào tử, M- Ti thể, HN- Nhân vật chủ.
3.3. Xét nghiệm PCR và qPCR
Các mẫu tôm thu thập từ nhóm thử nghiệm được kiểm tra EHP, kết quả dương tính với EHP sau ngày cảm nhiễm thứ 7. Trong khi các mẫu tôm từ nhóm đối chứng lại âm tính với EHP trong mọi khoảng thời gian. Trong nhóm thử nghiệm, tải lượng EHP được quan sát là tối đa ở ngày cảm nhiễm thứ 15 với (7,88 × 106 ± 2,93 × 106), tiếp theo là ngày thứ 30 (2,25 × 106 ± 7,64 × 105), thứ 90 (9,50 × 105 ± 4,51 × 105), và thứ 60 (7,71 × 105 ± 6,96 × 105) (Hình 3).
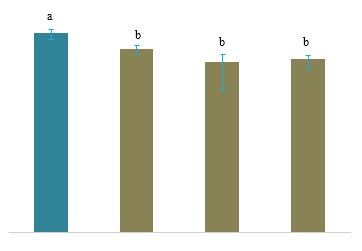
Hình 3. Tải lượng EHP của tôm được cảm nhiễm ở các khoảng thời gian khác nhau, sau ngày 15, 30, 60 và 90 (giá trị trung bình ± SD, n = 3). Các chữ cái trên hình mô tả ý nghĩa thống kê ở P <0,05.
3.4. Phân tích enzyme tiêu hóa và sinh hóa
Hoạt động của enzyme tiêu hóa α- amylase trong HP của tôm được cảm nhiễm thấp hơn đáng kể (P <0,05) tại mọi khoảng thời gian so với tôm đối chứng. Tương tự, các hoạt động của enzyme lipase trong HP ở nhóm cảm nhiễm cũng thấp đáng kể (P <0,05) ở mọi khoảng thời gian (Hình 4). Mức triglyceride của tôm cảm nhiễm EHP ở cả HP và hemolymph trong mọi khoảng thời gian đều giảm đáng kể (P <0,05) so với nhóm đối chứng. Tổng số protein trong HP giảm đáng kể (P <0,05) ở ngày cảm nhiễm thứ 30, 60 và 90, trong khi ở hemolymph, tổng số protein thấp đáng kể (P <0,05) ở ngày cảm nhiễm thứ 15 và 30. Mức cholesterol trong HP của tôm ở nhóm cảm nhiễm giảm đáng kể (P <0,05) ở ngày thứ 30 và 60, không có sự thay đổi đáng kể ở các khoảng thời gian khác trong HP và hemolymph. Mức glucose của của nhóm cảm nhiễm EHP thấp đáng kể (P <0,05) ở ngày cảm nhiễm thứ 30 và 60 trong HP và ngày thứ 15, 30 và 60 trong hemolymph. Nồng độ alanine aminotransferase (ALT) tăng đáng kể (P <0,05) ở ngày cảm nhiễm thứ 15 và 30 trong HP, và ngày thứ 30 trong hemolymph, nhưng không đáng kể ở các khoảng thời gian khác. Đồng thời, aspartase transferase (AST) không có thay đổi đáng kể (P <0,05) trong cả HP và hemolymph ở bất kỳ khoảng thời gian nào (Hình 5).
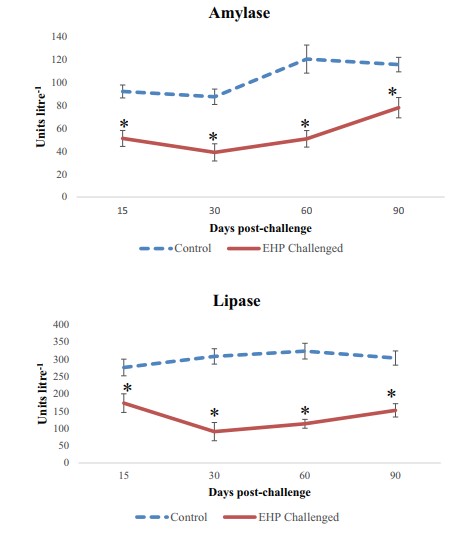
Hình 4. Hoạt động của enzym α-amylase (A) và lipase (B) trong HP của nhóm cảm nhiễm EHP ở ngày thứ 15, 30, 60 và 90 (trung bình ± SD, n = 3). Ký hiệu * mô tả ý nghĩa thống kê tại P <0,05.
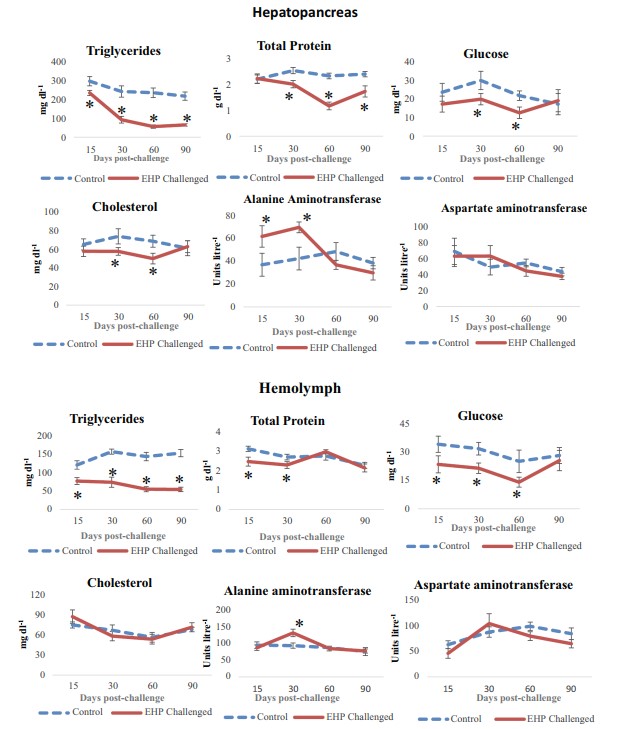
Hình 5. Triglyceride (TG), tổng số protein (TP), glucose (Glu), cholesterol (CL), alanine aminotransferase (ALT), aspartate aminotransferase (AST) hoạt động trong HP và hemolymph ở ngày cảm nhiễm thứ 15, 30, 60 và 90 (giá trị trung bình ± SD, n = 3). Ký hiệu * mô tả ý nghĩa thống kê tại P <0,05.
3.5. Phân tích các enzym miễn dịch và tổng số hemocyte (THC)
Mức ALP thấp đáng kể (P <0,05) ở ngày cảm nhiễm thứ 30, 60 và 90 và không đáng kể (P <0,05) ở ngày cảm nhiễm thứ 15 trong hemolymph. Hoạt động của catalase đã giảm đáng kể (P <0,05) trong hemolymph ở tất cả các ngày cảm nhiễm 15, 30, 60 và 90. Giá trị GGT đã giảm đáng kể (P <0,05) ở ngày cảm nhiễm thứ 15, 30, 60 và 90 trong hemolymph, khi so sánh với nhóm đối chứng. Do đó, giá trị T-AOC và SOA của hemolymph trong nhóm cảm nhiễm đã giảm đáng kể (P <0,05) ở tất cả các ngày so với nhóm đối chứng (Hình 6). Hoạt động của enzyme phenoloxidase trong hemolymph ở nhóm cảm nhiễm đã giảm đáng kể (P <0,05) ở ngày thứ 15, 60, 90 và tăng lên ở ngày thứ 30 nhưng không đáng kể (Hình 6). Do đó, tổng số hemocyte (THC) của nhóm cảm nhiễm thấp hơn đáng kể (P <0,05) so với nhóm đối chứng ở tất cả các khoảng thời gian 15, 30, 60 và 90 (Hình 7).

Hình 6. Alkaline phosphatase (ALP), catalase, γ- glutamyl transferase (GGT), superoxide anion (SOA), tổng khả năng chống oxy hóa (T-AOC) và các hoạt động của phenoloxidase trong hemolymph ở ngày cảm nhiễm thứ 15, 30, 60 và 90 (giá trị trung bình ± SD, n = 3). Ký hiệu * mô tả ý nghĩa thống kê ở P <0,05.
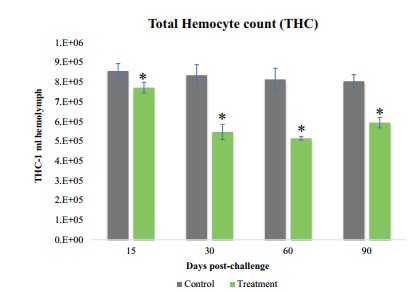
Hình 7. Tổng số hemocyte của tôm ở nhóm đối chứng và nhóm cảm nhiễm EHP ở ngày thứ 15, 30, 60 và 90 (giá trị trung bình ± SD, n = 3). Ký hiệu * mô tả ý nghĩa thống kê ở P <0,05.
3.6. Hiệu suất tăng trưởng
Sau 90 ngày thử nghiệm, trọng lượng trung bình của tôm ở nhóm cảm nhiễm (12,17 ± 0,80 g) thấp hơn đáng kể (P <0,05) so với nhóm đối chứng (19,27 ± 0,57 g) (Hình 8A). Mức tăng trọng ở nhóm cảm nhiễm là 8,70 ± 0,91 g, trong khi nhóm đối chứng là 15,78 ± 0,53 g. Tốc độ tăng trưởng cụ thể của nhóm cảm nhiễm (1,39 ± 0,11) thấp hơn đáng kể (P <0,05) so với nhóm đối chứng (1,89 ± 0,03). Tốc độ tăng trưởng trung bình hàng ngày của nhóm cảm nhiễm là 96,72 ± 10,2 mg, trong khi nhóm đối chứng là 175,34 ± 5,9 mg. Hệ số chuyển đổi thức ăn (FCR) của nhóm cảm nhiễm (3,01 ± 0,29) cao hơn đáng kể (P <0,05) so với nhóm đối chứng (1,64 ± 0,05). Ngoài ra, chỉ số gan (HSI) của nhóm cảm nhiễm (3,57 ± 0,23) thấp hơn đáng kể (P <0,05) so với nhóm đối chứng (4,18 ± 0,39). Tỷ lệ sống của nhóm cảm nhiễm (71,1 ± 11,70), thấp hơn nhóm đối chứng (89,9 ± 5,77) nhưng không đáng kể (P <0,05) (Bảng 1). Trong quá trình thử nghiệm, lượng thức ăn tiêu được quan sát thấy thấp sau ngày cảm nhiễm thứ 8 và dao động trong suốt thử nghiệm ở nhóm cảm nhiễm EHP khi so sánh với nhóm đối chứng. Trong đường cong tăng trưởng, tốc độ tăng trưởng của nhóm đối chứng và nhóm cảm nhiễm không có sự khác biệt đáng kể sau ngày cảm nhiễm thứ 15 nhưng được quan sát là có sự thay đổi đáng kể (P <0,05) từ ngày cảm nhiễm thứ 30 đến kết thúc thử nghiệm (Hình 8B). Tuy nhiên, sự lột xác chậm và tỷ lệ chết được quan sát thấy ở ngày thứ 15 trong nhóm cảm nhiễm.
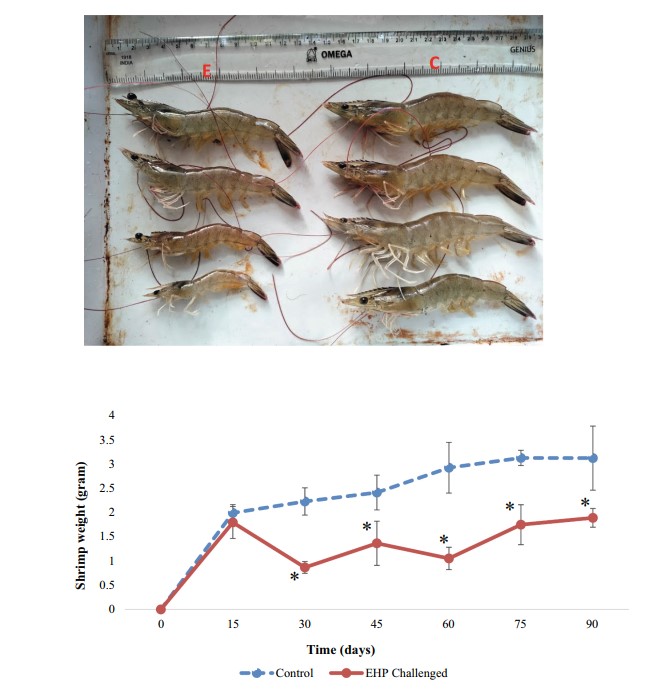
Hình 8. A- Tôm cảm nhiễm EHP được quan sát thấy chậm lớn và thay đổi kích thước sau 90 ngày, tôm đối chứng (C) được quan sát không có bất kỳ sự chậm lớn và thay đổi kích thước nào sau 90 ngày. B- Đường cong tăng trưởng của cả tôm đối chứng và tôm cảm nhiễm EHP sau 90 ngày. Ký hiệu * mô tả ý nghĩa thống kê tại P <0,05.
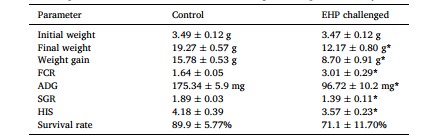
Bảng 1: Hiệu suất tăng trưởng của tôm đối chứng và tôm nhiễm EHP sau 90 ngày.
Ký hiệu chỉ số trên * thể hiện ý nghĩa thống kê P <0,05.
4/ Thảo luận
Bệnh HPM do EHP gây ra không gây chết hàng loạt nhưng được báo cáo là làm tôm chậm lớn / thay đổi kích thước. Điều này dẫn đến thiệt hại nghiêm trọng về kinh tế trong việc nuôi tôm và làm cho dịch bệnh trở nên nguy hiểm hơn đối với việc nuôi tôm bền vững. Trong nghiên cứu này, để điều tra mối tương quan giữa sự chậm lớn và EHP, tôm được cảm nhiễm EHP và tôm đối chứng được nuôi trong 90 ngày, và các mẫu được thu thập trong các khoảng thời gian khác nhau để đánh giá các phản ứng tiêu hóa, sinh lý, miễn dịch và tăng trưởng.
Gan tụy (HP) là cơ quan tiêu hóa quan trọng của động vật giáp xác, có thể thực hiện các chức năng của cả gan và tuyến tụy của động vật có vú. HP cần thiết cho quá trình tiêu hóa thức ăn, hấp thụ, vận chuyển, tích trữ năng lượng dự trữ và một số hoạt động trao đổi chất quan trọng (Wang và cộng sự, 2014). Do đó, HP là cơ quan chủ đích của vi khuẩn EHP ở tôm. Trong quá trình nghiên cứu, kiểm tra mô học cho thấy các ống HP bị hoại tử. Ngoài ra, còn có sự bong tróc và hoại tử của và các tế bào biểu mô (tế bào B, tế bào R, tế bào E), giai đoạn đầu và cuối của plasmodial, bào tử trưởng thành tự do, và sporoblast trong tế bào chất biểu mô và lòng ống HP của tôm cảm nhiễm với EHP ở mọi khoảng thời gian. Kết quả so sánh cho thấy hoại tử nghiêm trọng ở ngày thứ 30 sau khi cảm nhiễm. Tuy nhiên, tải lượng EHP được phát hiện là tối đa (106 bản sao/ ng DNA) ở ngày thứ 15 và đạt tới 105 bản sao/ ng DNA ở ngày thứ 90 sau khi cảm nhiễm. Kết quả kiểm tra TEM cho thấy sự hiện diện của các ti thể vật chủ xung quanh EHP. Các ti thể vật chủ thường bao quanh vi bào tử trùng để tạo điều kiện thuận lợi cho việc hấp thụ ATP cho sự phát triển của ký sinh trùng (Boakye và cộng sự, 2017; Williams và cộng sự, 2014). Ngoài ra, chỉ số gan của tôm cảm nhiễm thấp hơn đáng kể so với nhóm đối chứng. Do đó, HP đã bị hoại tử nghiêm trọng bởi EHP sau ngày cảm nhiễm thứ 15.
α-amylase là một enzyme tiêu hóa quan trọng trong chuyển hóa carbohydrate và xúc tác quá trình thủy phân carbohydrate thành oligosaccharide (Guillaume và cộng sự, 1999). Enzyme lipase tiêu hóa lipid từ thức ăn và lipid từ nguồn dự trữ trong lúc đói, đồng thời đóng một vai trò quan trọng trong chuyển hóa lipid (Guillaume và cộng sự, 1999). Trong nghiên cứu này, hoạt động của α-amylase và lipase đã giảm đáng kể trong HP của nhóm cảm nhiễm ở mọi khoảng thời gian. Hoạt động của enzyme α-amylase và lipase thấp cho thấy quá trình tiêu hóa và chuyển hóa carbohydrate và lipid của vật chủ không đúng cách. Tương tự, Duan và cộng sự (2021) báo cáo rằng các gen liên quan đến chuyển hóa carbohydrate và lipid đã được điều chỉnh để chống lại sự lây nhiễm EHP. Ngoài ra, quá trình chuyển hóa năng lượng của tôm được mô tả là bị thay đổi đáng kể sau khi nhiễm EHP (Ning và cộng sự, 2019; Yang và cộng sự, 2021). Tương tự, nhiễm trùng vi bào tử trùng ở ong mật cũng đã làm thay đổi biểu hiện gen liên quan đến carbohydrate và axit amin chuyển hóa (Pan và cộng sự, 2018).
Đối với các biến số chuyển hóa, mức TG thấp hơn ở cả HP và hemolymph của tôm được cảm nhiễm (ngày thứ 15, 30, 60, 90). Triglyceride là năng lượng dự trữ cần thiết cho tôm; sự giảm nồng độ chất béo trung tính cho thấy rối loạn chuyển hóa lipid và tăng nhu cầu trao đổi chất (Gopinath, 2006; Mercier và cộng sự, 2006). Tương tự, Chen và cộng sự (2011) đã báo cáo nồng độ chất béo trung tính giảm đáng kể và liên tục ở tôm nhiễm WSSV. Protein là chất nền cơ bản cần thiết cho sự tăng trưởng và trao đổi chất; sự giảm TP huyết thanh (sau ngày cảm nhiễm thứ 15 và 30) biểu thị sự giảm sự phát triển của tế bào và hoạt động trao đổi chất, đòng thời chỉ ra sự phát triển của bệnh. Ngoài ra, mức TP giảm trong HP (sau ngày cảm nhiễm thứ 30, 60, 90) có thể tương quan với tổn thương tế bào gan (Gopinath, 2006). Cholesterol là tiền chất của các hormone steroid và chịu trách nhiệm cho việc cân bằng nội môi, lột xác và đại diện cho các tình trạng stress (Gopinath, 2006; Kumar và cộng sự, 2018). Sự giảm mức cholesterol (sau ngày cảm nhiễm thứ 30 và 60) trong HP cho thấy tôm đang bị stress cũng như chậm lột xác và tăng trưởng. Ngoài ra, việc giảm glucose trong HP (sau ngày cảm nhiễm thứ 30, 60) và trong hemolymph (sau ngày cảm nhiễm thứ 15, 30, 60) cho thấy sự tổn thương trong HP. Tương tự, nồng độ glucose giảm có tương quan với rối loạn sinh lý tôm trong việc chống lại sự lây nhiễm WSSV (Chen và cộng sự, 2011). Nồng độ ALT tăng cao trong HP (sau ngày cảm nhiễm thứ 15 và 30) và trong hemolymph (sau ngày cảm nhiễm thứ 30) được quan sát thấy ở nhóm cảm nhiễm, đồng thời cũng cho thấy sự tổn thương trong HP (Pan và cộng sự, 2003). Tương tự, mức ALT được quan sát thấy là gia tăng đáng kể ở tôm nhiễm EHP (Santhoshkumar và cộng sự, 2017) và WSSV (Mohankumar và Ramasamy, 2006), đồng thời cũng liên quan đến tổn thương mô. Nosema ceranae cũng được cho là gây ra các tác động đáng kể đến nhiều chức năng sinh lý ở loài ong Apis mellifera (Va´vra và Lukeˇs, 2013)
Trong hệ thống miễn dịch của tôm, mức ALP đã giảm đáng kể ở cả HP (dữ liệu không được hiển thị) và hemolymph (sau ngày cảm nhiễm thứ 30, 60 và 90) trong nhóm cảm nhiễm. Sự tổn thương HP ở tôm có thể ức chế sự giải phóng ALP (Long và cộng sự, 2021). Tương tự, Duan và cộng sự, (2021) đã báo cáo sự điều hòa giảm của các gen ALP chống lại sự lây nhiễm EHP. Alkaline phosphatase đóng một vai trò quan trọng trong quá trình thực bào bằng cách loại bỏ nhóm phosphoryl khỏi mầm bệnh và dự trữ trong lysosome (Wang và cộng sự, 2019). Ngoài ra, các hoạt động của GGT đã giảm đáng kể ở những nhóm tôm cảm nhiễm. GGT cần thiết cho sự tổng hợp glutathione và đóng vai trò quan trọng trong hệ thống miễn dịch (Xu và cộng sự, 2019). Do đó, trong quá trình bảo vệ chống oxy hóa của tôm cảm nhiễm, mức độ hoạt động của CAT trong hemolymph thấp hơn đáng kể so với nhóm đối chứng. Ngoài ra, mức độ hoạt động T-AOC và SOA đã giảm đáng kể trong hemolymph của tôm được cảm nhiễm tại mọi thời khoảng thời gian. Hệ thống bảo vệ chống oxy hóa của tôm được kích hoạt trong những điều kiện khắc nghiệt để loại bỏ ROS, chống lại stress oxy hóa và ngăn ngừa tổn thương DNA, lipid và protein (Xu và cộng sự, 2018). Hoạt động của enzym PO đã giảm đáng kể trong hemolymph ở nhóm cảm nhiễm EHP (sau ngày cảm nhiễm thứ 15, 30 và 90). Hệ thống kích hoạt phenoloxidase thực hiện melanization, một phản ứng miễn dịch bẩm sinh quan trọng chống lại sự phát hiện mầm bệnh (Amparyup và cộng sự, 2013). Tương tự, Duan và cộng sự (2021) đã quan sát thấy rằng các gen phenoloxidase và antioxidant được điều hòa để chống lại sự lây nhiễm EHP. Ở ong mật, tất cả các gen miễn dịch tiềm năng và peptit chống vi khuẩn đã được điều chỉnh để chống lại sự lây nhiễm vi bào tử trùng (Pan và cộng sự, 2018). Do đó, hệ thống miễn dịch không đặc hiệu và khả năng bảo vệ chống oxy hóa của tôm bị ảnh hưởng bởi nhiễm EHP.
Tác động của EHP lên gan tụy của tôm ảnh hưởng đến tiêu hóa, sinh lý, trao đổi chất và hệ thống miễn dịch. Sau khi tác động đến sinh lý và trao đổi chất, chúng làm giảm đáng kể sự tăng trưởng của tôm. Tương tự, nhiễm EHP được cho là làm rối loạn khả năng tiêu hóa, hấp thụ và vận chuyển (Yang và cộng sự, 2021). Trong nghiên cứu này, lượng thức ăn tiêu thụ thấp được quan sát thấy ở nhóm cảm nhiễm EHP sau ngày cảm nhiễm thứ 8. Do đó, FCR của nhóm cảm nhiễm cao hơn và tăng trọng trung bình hàng ngày của tôm ở nhóm này giảm đáng kể. Tương tự, tốc độ tăng trưởng hàng ngày được quan sát thấy là thấp trong các ao tôm bị ảnh hưởng bởi EHP (Dewangan và cộng sự, 2021). Tỷ lệ sống của nhóm cảm nhiễm thấp hơn nhóm đối chứng nhưng không đáng kể. Do đó, với dữ liệu trong thử nghiệm này, ước tính thiệt hại về sản lượng do nhiễm EHP trong ao một ha (với mật độ thả 40 con/m2) sẽ là 3,44 tấn / ha.
EHP thiếu ty thể (Tourtip và cộng sự, 2009), và do đó không thể sản xuất ATP thông qua quá trình phosphoryl hóa oxy hóa, và phụ thuộc nhiều vào vật chủ để cung cấp năng lượng. Vi bào tử trùng được biết là có ảnh hưởng đến sự trao đổi chất của vật chủ và sử dụng các chất chuyển hóa của vật chủ để tạo điều kiện thuận lợi cho sự sinh sôi của ký sinh trùng. Ngoài ra, chúng cũng được báo cáo là có thể điều chỉnh sinh lý vật chủ và làm suy yếu hệ thống phòng thủ miễn dịch của vật chủ (Va´vra và Lukeˇs, 2013). Với nghiên cứu này, rõ ràng là nhiễm EHP đã điều chỉnh và ảnh hưởng đến sinh lý, sự trao đổi chất và hệ thống miễn dịch của tôm. Vi bào tử trùng chiếm ưu thế trong thử nghiệm sống chung bằng cách nhắm mục tiêu vào cơ quan chủ đích, có khả năng phục hồi cao để sản sinh liên tục các bào tử (Va´vra và Lukeˇs, 2013). HP của tôm có khả năng phục hồi và khả năng tự điều chỉnh cao (Sathish Kumar và cộng sự, 2022; Wang và cộng sự, 2019). Khả năng phục hồi này có thể bù đắp cho sự tổn thương bởi EHP ở một mức độ nào đó. Ngoài ra, có thông tin cho rằng khả năng phòng thủ của vật chủ có thể không đủ để loại bỏ hoàn toàn sự hiện diện vi bào tử trùng (Weiss, 2014). Do đó, các động vật bị nhiễm vi bào tử trùng hoạt động tương đối bình thường, và vi bào tử trùng được báo cáo là có thể làm chậm tỷ lệ chết của vật chủ (Va´vra và Lukeˇs, 2013). Nghiên cứu này quan sát thấy rằng tỷ lệ sống của tôm (71,1%) sau khi nhiễm EHP có tốc độ tăng trưởng dưới mức tối ưu đến 90 ngày.
5/ Kết luận
Trong nghiên cứu này, ảnh hưởng của EHP đến sinh lý, trao đổi chất và hệ thống miễn dịch ở các khoảng thời gian khác nhau đã được nghiên cứu đồng thời với sự tăng trưởng của tôm thẻ chân trắng P. vannamei. EHP gây tổn thương nghiêm trọng cho HP của tôm và ảnh hưởng đến quá trình tiêu hóa, bài tiết, và hấp thụ. Tác động của EHP đối với HP ảnh hưởng đáng kể đến sinh lý, trao đổi chất và tăng trưởng của tôm. Tuy nhiên, những con tôm được cảm nhiễm vẫn sống sót khi bị nhiễm EHP. Do đó, chất kích thích miễn dịch, chất phụ gia phục hồi HP và chất xử lý EHP có thể hữu ích để phục hồi sinh lý, trao đổi chất, hệ thống miễn dịch và tăng trưởng. Kết luận, nhiễm EHP không gây chết hàng loạt mà ảnh hưởng nghiêm trọng đến khả năng tiêu thụ thức ăn, tăng trưởng, FCR, cuối cùng là làm tăng chi phí sản xuất và gây thiệt hại nặng nề về kinh tế trong nuôi tôm. Ngoài ra, nghiên cứu này sẽ hữu ích trong việc hiểu vòng đời của EHP và tiêu chuẩn hóa các phương pháp phòng và trị để kiểm soát EHP.
Theo: T. Sathish Kumar, P. Ezhil Praveena, T. Sivaramakrishnan, J. Joseph Sahaya Rajan, M. Makesh, K.P. Jithendran
Từ khóa: Enterocytozoon hepatopenaei (EHP), Bệnh nhiễm vi bào tử trùng (HPM), Sinh lý tôm, Tăng trưởng chậm, Penaeus vannamei
Biên dịch: Huyền Thoại – Tôm Giống Gia Hóa Bình Minh
“Tôm Giống Gia Hóa – Chìa Khóa Thành Công”
Xem thêm:
- Ngâm Với Eugenol Có Thể Giảm Thiểu Các Phản Ứng Căng Thẳng Ở Tôm Nuôi Khi Vận Chuyển
- Biofilm Và Các Biện Pháp Kiểm Soát Chúng (Phần 1)
- Axit Hữu Cơ Và Muối Vi Nang Có Lợi Trong Sản Xuất Tôm Thẻ Chân Trắng

 English
English